Saúde
Saúde autoriza municípios a vacinarem adolescentes de 12 anos com comorbidade
Campo Grande News
18 de Junho de 2021 - 13:28
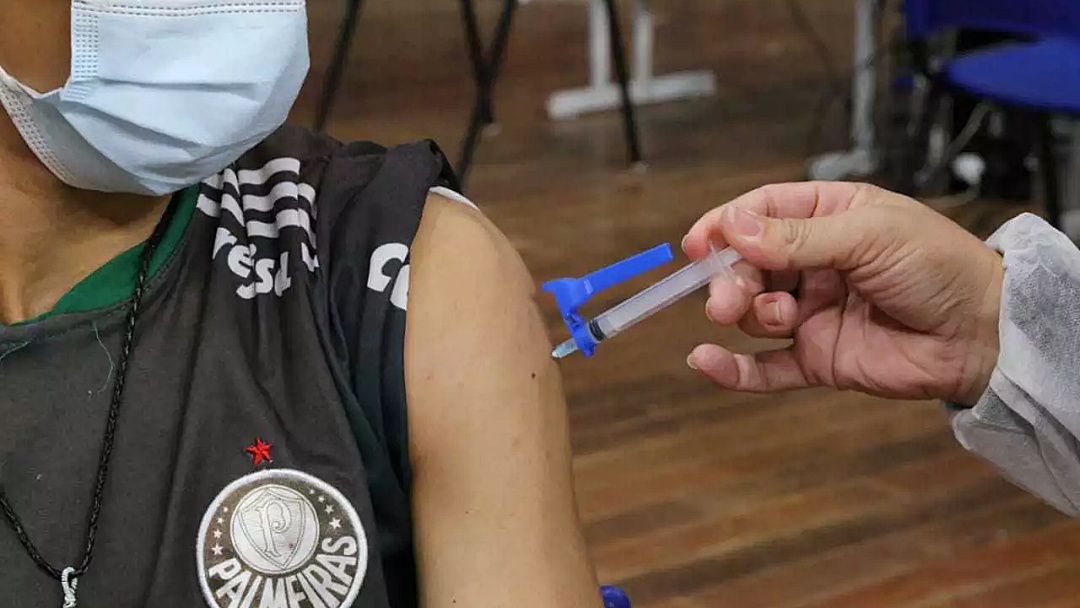
Municípios de Mato Grosso do Sul foram autorizados pela SES (Secretaria Estadual de Saúde) a vacinar adolescentes, acima de 12 anos, que tenham algum tipo de comorbidade, com imunizantes da Pfizer. Segundo publicação em Diário Oficial do Estado, as cidades terão de utilizar vacinas que façam parte dos 70% do quantitativo destinado a imunização relacionada à faixa etária.
Nesta semana, conforme apurado pelo Campo Grande News, a Sesau (Secretaria Municipal de Saúde) abriu pré-cadastro de adolescentes para serem imunizados contra a covid em Campo Grande. Alguns estados brasileiros como o Ceará também passaram a fazer esse levantamento. Nesses casos, não há previsão de quando esse grupo será vacinado.
No município de Betim, em Minas Gerais, a prefeitura decidiu vacinar estudantes sem comorbidade entre 12 e 14 anos na quarta-feira (16), com objetivo de retomar aulas públicas semipresenciais em agosto, mas a decisão foi barrada pelo TJMG (Tribunal de Justiça de Minas Gerais), que obrigou o município a comprovar que havia vacinado todos os grupos prioritários incluídos no PNI (Plano Nacional de Imunização) e todos os adultos acima de 18 anos sem comorbidade.
Já o município de Cacoal, em Rondônia, incluiu jovens com comorbidades no calendário de vacinação, nesta semana, e a imunização segue acontecendo. A reportagem perguntou à SES qual estratégia deverá ser adotada pelos municípios sul-mato-grossenses, bem como quais critérios foram utilizados para essa decisão, mas não foi respondida até a publicação desta matéria.
Comorbidades - A publicação feita pelo executivo estadual estabelece que podem ser vacinados adolescentes "desde que, portadores de alguma das comorbidades descritas no quadro 2 do Plano Nacional de Operacionalização da Vacinação Contra a Covid-19, em vigor". São elas:
- Diabetes mellitus;
- Pneumopatias crônicas graves;
- Hipertensão Arterial Resistente (HAR);
- Hipertensão arterial estágio 3;
- Hipertensão arterial estágios 1 e 2 com lesão em órgão-alvo e/ou comorbidade;
- Insuficiência cardíaca (IC);
- Cor-pulmonares e Hipertensão pulmonar;
- Cardiopatia hipertensiva;
- Síndromes coronarianas;
- Valvopatias; Miocardiopatias e Pericardiopatias;
- Doenças da Aorta, dos Grandes Vasos e Fístulas arteriovenosas;
- Arritmias cardíacas;
- Cardiopatias congênita no adulto;
- Próteses valvares e Dispositivos cardíacos implantados;
- Doença cerebrovascular;
- Doença renal crônica;
- Imunossuprimidos;
- Hemoglobinopatias graves;
- Obesidade mórbida Índice de massa corpórea (IMC) ≥ 40;
- Cirrose hepática.
Conforme dados da SES, das mais de 7 mil mortes por coronavírus, 13 eram pacientes com menos de 19 anos. Desses, a maioria (10) tinha ao menos um tipo de comorbidade como doenças pulmonares, cardíacas, diabetes ou obesidade.
Autorização federal - Na última sexta-feira (11), a Anvisa (Agência Nacional de Vigilância Sanitária) já havia autorizado uso da vacina da Pfizer para adolescentes com 12 anos ou mais, depois de pedido feito em 13 de maio. Com essa decisão, a bula da vacina passou a indicar a nova faixa etária, que antes era para pessoas com 16 anos ou mais, e é a única entre as autorizadas no Brasil com indicação para menores de 18 anos.
Segundo o órgão, a medida foi aprovada depois que a empresa estadunidense apresentou estudos que indicaram segurança e eficácia da vacina para este grupo. Os estudos foram desenvolvidos fora do país e analisados pela Anvisa. O uso do imunizante em adolescentes entre 12 e 15 anos já é permitido nos Estados Unidos e na Europa desde maio, com aprovação da FDA (Agência de Alimentos e Medicamentos), e da EMA (Agência Europeia de Medicamentos), feitas depois de estudos que garantiram segurança e eficácia.
Crianças - Desde o começo de mês, a Pfizer tem feito avanço nos testes da vacina contra a covid-19 em crianças de cinco a 11 anos, mas ainda não foram concluídos. Caso seja avaliado positivamente nos testes, o imunizante ainda passará por uma série de análises de segurança e ainda vão precisar de aprovação da Anvisa para serem aplicados em território brasileiro.
Essas análises, feitas em parceria com o laboratório alemão BioNTech, começaram no final de março, envolvendo 4,5 mil crianças de seis meses a 11 anos nos Estados Unidos, Finlândia, Polônia e Espanha. Posteriormente, a Pfizer ainda considera avaliar a vacina para crianças com menos de seis meses.